I ett infall av saknad av min tidigare karriär som först kemilärare och sedan forskare kom jag på att jag skulle förklara vetenskapen bakom några av våra överlevnadsprodukter som bygger på kemiska principer.
Engångshandvärmare
Handvärmare innehåller en påse som påminner om en stor tepåse. Påsen är oftast fylld med järnpulver, vatten, aktivt kol, träpulver, koksalt och vermikulit. Järnet är ger värme, övriga ämnen i påsen har som uppgift att katalysera reaktionen, fördela värmen och göra så att den släpps ut i lagom takt.
När det finkorniga järnpulvret kommer i kontakt med syret i luften oxideras det till en blandning av olika järnoxider. Precis som många redox-reaktioner är denna reaktion exoterm, dvs. den avger värme. Temperaturen kan bli upp till 70 grader och håller i 4-12 timmar, beroende på hur stor påsen är.
X Fe + Y/2 O2 → FeXOY [+ värme]
Engångshandvärmarna kan bara användas en gång, men det kan gå att stoppa uppvärmningen genom att stoppa ner den aktiverade påsen i en liten blixtlåspåse, så att den inte får mer syre. När den tas ut ur blixtlåspåsen börjar förhoppningsvis det kvarvarande järnpulvret reagera och påsen blir varm igen. När en engångshandvärmare är förbrukad kan den kastas i soporna, inget av innehållet är giftigt.
Återanvändningsbar handvärmare
Återanvändningsbara handvärmare går däremot att använda många gånger. De utgörs av påsar av tjock plast som innehåller en väldigt koncentrerad vattenlösning av saltet natriumacetat. En så koncentrerad lösning kallas övermättad och i en sådan lösning borde egentligen kristaller börja bildas. Men för att kristallisationen ska kunna sätta igång behöver kristallerna något att växa på. Just natriumacetat är ett salt som klarar väldigt hög övermättnad innan det börjar kristallisera.
I handvärmaren finns en liten metallplatta som går att knäcka till med fingrarna. Då släpper den mikroskopiska metallflisor som natriumacetatet kan fastna på och börja bilda kristaller. Kristallisationen är väldigt snabb och den kemiska energin som finns lagrad släpps ut i form av värme. en återanvändningsbar handvärmare blir inte lika varm som en engångshandvärmare och håller heller inte värmen så länge.
NaOAc(aq) → NaOAc(s) [+ värme]
När handvärmaren svalnat kan man lägga den i kokande vatten och när påsen uppnår en viss temperatur kommer saltkristallerna att lösa sig igen. Handvärmaren kan då användas igen. Om man kokar den strax innan man ska gå ut så kan man värma sig på den två gånger utan att koka den emellan eftersom den håller värmen från kokningen i någon timme. När en återanvändningsbar handvärmare efter många användningar till slut slutar fungera, kan den kastas i soporna. Natriumacetat är inte giftigt.
Värmepåse till mjukkonserver
I en värmepåse stoppar man ner en oöppnad mjukkonserv (eller en vanlig konservburk) och häller i en liten mängd vatten. Påsen blir då 70-80 grader varm under 15-20 minuter och värmer upp konservens innehåll på 5-10 minuter. Det är ett smidigt sätt att få en varm måltid, utan att bära med sig ett stormkök med bränsle.
Värmepåsar innehåller antingen kalciumhydroxid eller magnesiumpulver, järnpulver, kiseldioxid och koksalt. Varje värmepåse går bara att använda en gång. Förbrukade värmepåsar går att slänga i soporna, men innehållet är lite frätande, så var försiktig med hanteringen.
Ca(OH)2(s) + H2O → Ca(OH)2(aq) [+ värme]
Mg + 2H2O → Mg(OH)2 + H2 [+ värme]
Syreabsorbenter
Syreabsorbenter används framför allt tillsammans med mylarpåsar, för att fånga upp syret som finns kvar i de förslutna påsarna så att man får en helt syrefri miljö, vilket förlänger hållbarheten på många livsmedel.
Syreabsorbenter har ungefär samma innehåll som engångshandvärmare (järn, kol och koksalt) och blir varma när syret reagerar med järnet. De fungerar därför inte så bra ihop med vissa livsmedel, till exempel strösocker som kan smälta och klumpa ihop. Syreabsorbenterna suger bara upp syret i luften, inte kvävet (som utgör 78%) så det blir inte vakuum i påsarna
Vattenreningstabletter
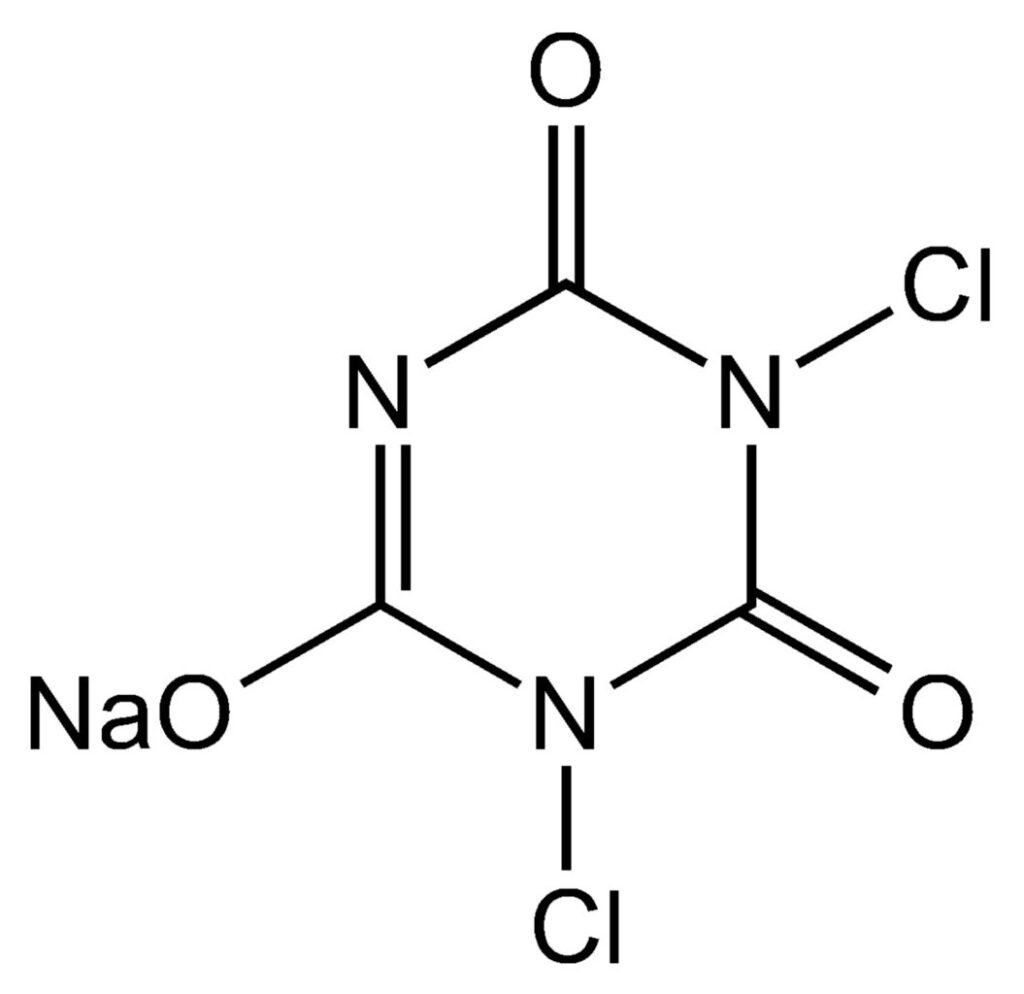
Vattenreningstabletter innehåller någon typ av kemikalie som oxiderar sönder virus, bakterier och parasiter. Den vanligaste typen innehåller klor, men bundet i form av natriumdikloroisocyanurat (troclosen natrium). Tabletter med natriumdikloroisocyanurat är stabila och går att lagra i flera år. När man stoppar i en tablett i vatten frigörs kloret långsamt och i jämn takt. Klor är ett väldigt starkt oxidationsmedel och reagerar med ytan på virus, bakterier och protozoer så att de oskadliggörs.
Vattenreningstabletter är självklart skadliga för vattenlevande organismer, det är liksom tanken med dem. Natriumdikloroisocyanurat är frätande, så man ska hantera tabletterna försiktigt och förstås inte äta dem.
Kolfilter
Kolfilter fungerar genom att de innehåller små kolpartiklar med extremt stor yta, det är det som kallas aktivt kol. På denna yta kan vissa kemikalier fastna när man leder en gas eller vattenlösning över den (kallas adsorbtion, inte att förväxla med absorption). I första hand är det organiska molekyler (ofta sådana som ger lukt, smak eller färg) och vissa metaller som fastnar, men reningen är långt ifrån hundraprocentig. Kolfilter blir mättade efter en tid och behöver bytas regelbundet. Även kolfilter som inte används blir dåliga om de inte ligger i lufttäta förpackningar.
Vattenfilter
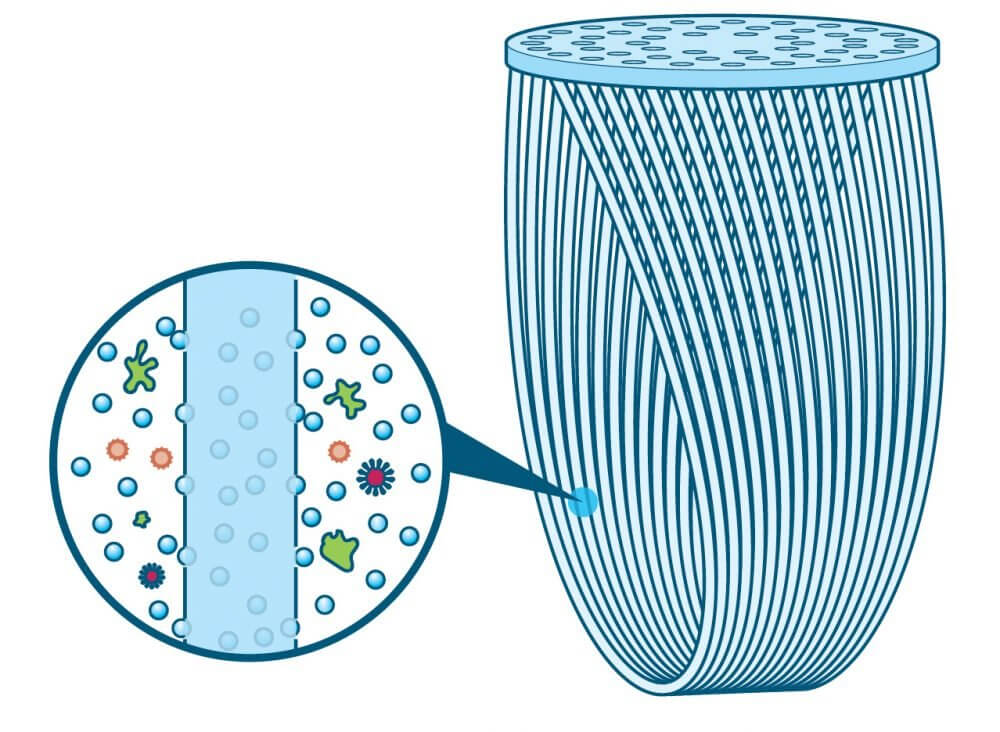
Mikrobiologiska vattenreningsfilter fungerar som en sil, med noga kontrollerad storlek på hålen. Filtren är oftast gjorda av keramik eller textil och hur stora hålen är beror på vad men vill få bort från vattnet. Bakterier och parasiter är större än 1 mikrometer (miljondels meter) och vanliga vattenreningsfilter brukar ha porer som är 0,1-0,2 mikrometer.
Virus är däremot så små så de går igenom dessa filter (men det är normalt inga höga halter av virus i sjö- och flodvatten i Sverige om det inte går ut ett avlopp i närheten). Filter som klarar av att rena bort virus har porer som är så små som 0,02 mikrometer, vilket gör att vattnet rinner långsammare genom dessa filter än andra filter.
Frystorkad mat
Vid frystorkning sänker man lufttrycket till nära vakuum och sänker samtidigt temperaturen långt under fryspunkten. Det gör att i stort sett allt vatten försvinner genom att det först fryser till is och sedan sublimerar (går direkt från fast till gasform, utan att passera flytande form). Livsmedlet behåller då både form, färg och näringsvärde och när man tillsätter varmt vatten återfår man något som ligger ganska nära den ursprungliga maten i smak och konsistens.
Mylar
Mylar är ett flerskiktsmaterial som består av polyeten, aluminium och PET och skyddar mot solljus, fukt och syre. Detta gör att livslängden på livsmedel som är förpackade i mylar förlängs. Det innersta lagret i mylar utgörs av polyeten (även kallat polyetylen eller PE) är godkänt för kontakt med livsmedel och gör mylaren seg och motståndskraftig. Polyeten smälter vid ca 120 grader och det är detta lager som smälter när man svetsar ihop mylar.
Nästa lager utgörs av en väldigt tunn aluminiumfolie som förhindrar att ljus tränger igenom. Den är också ogenomtränglig för gaser, vilket gör att t.ex syre och lukter inte kan tränga igenom. Genom många andra typer av plast kan gasmolekyler vandra långsamt även om plasten är lufttät, men inte genom mylar.
Det tredje och yttersta lagret utgörs av en variant av polyetylentereftalat (PET, dvs plasten i läskflaskor) som kallas BoPET. Denna plast både flexibel och stark och reagerar inte så lätt med olika kemikalier. BoPET-lagret kan variera i tjocklek och det är det som gör att det finns olika tjocklekar på mylar. BoPET smälter vid ca 260 grader och smälter normalt inte när man svetsar igen mylar, utan det är polyetenlagret som gör det.Eftersom innerskiket tål över 100 grader så går det bra att hälla kokande vatten i mylarpåsarna, vilket man exempelvis gör när man tillagar portionspåsar med frystorkad mat.
Nödfiltar och nödsovsäckar av ”silverfolie”, så kallade ”space blankets”, är också tillverkade av mylar. Förutom att de är vind och vattentäta så gör aluminiumlagret att en stor del av kroppsvärmen reflekteras tillbaka mot kroppen.
Eldstål
Eldstål är en metallstav som ger ifrån sig gnistor om du skrapar på den med ett hårdare material. Eldstål kallas ofta på engelska för ferrocerium steel, och är tillverkade av en legering mellan flera sällsynta jordartsmetaller (vanligen cerium, lantan, neodym) och järn. Järninnehållet brukar bara runt 5%.







Mycket trevligt skrivet och förklarat på ett funktionellt sätt med en,i sammanhanget, rationell nivå av vetenskap!